Eliminating base-editor-induced genome-wide and transcriptome-wide off-target mutations
作者: 杨力 期刊:Nature Cell Biology 时间:2021.5
Abstract
CRISPR-Cas9与胞苷脱氨酶( cytidine deaminases )的融合导致了能够进行可编程C-to-T编辑的碱基编辑器( base editors,BEs),该编辑器具有临床应用潜力,但存在脱靶(off-target ,OT)突变。这里,作者使用一个可剪切的脱氧胞苷脱氨酶抑制剂(dCDI)结构域构建了一个 变形式BE (tBE)系统,该系统仅在全基因组和转录组范围的OT突变的背景水平上就能诱导高效的编辑。 产生后,tBE在OT位点与可裂解dCDI融合保持不活跃状态,因此消除了意外突变。 当结合在目标位点时,tBE被转化以切断dCDI结构域,并催化靶向脱氨基以进行精确的碱基编辑 。 通过双腺相关病毒(AAV)系统导入小鼠后,tBE系统在Pcsk9中创建了一个提前终止密码子,显著降低了血清中Pcsk9,导致总胆固醇下降~ 30-40%。 tBE的开发建立了一种高度特异性的碱基编辑系统,其体内疗效具有治疗应用的潜力。
Fig. 1 | identification of dCDi domains.
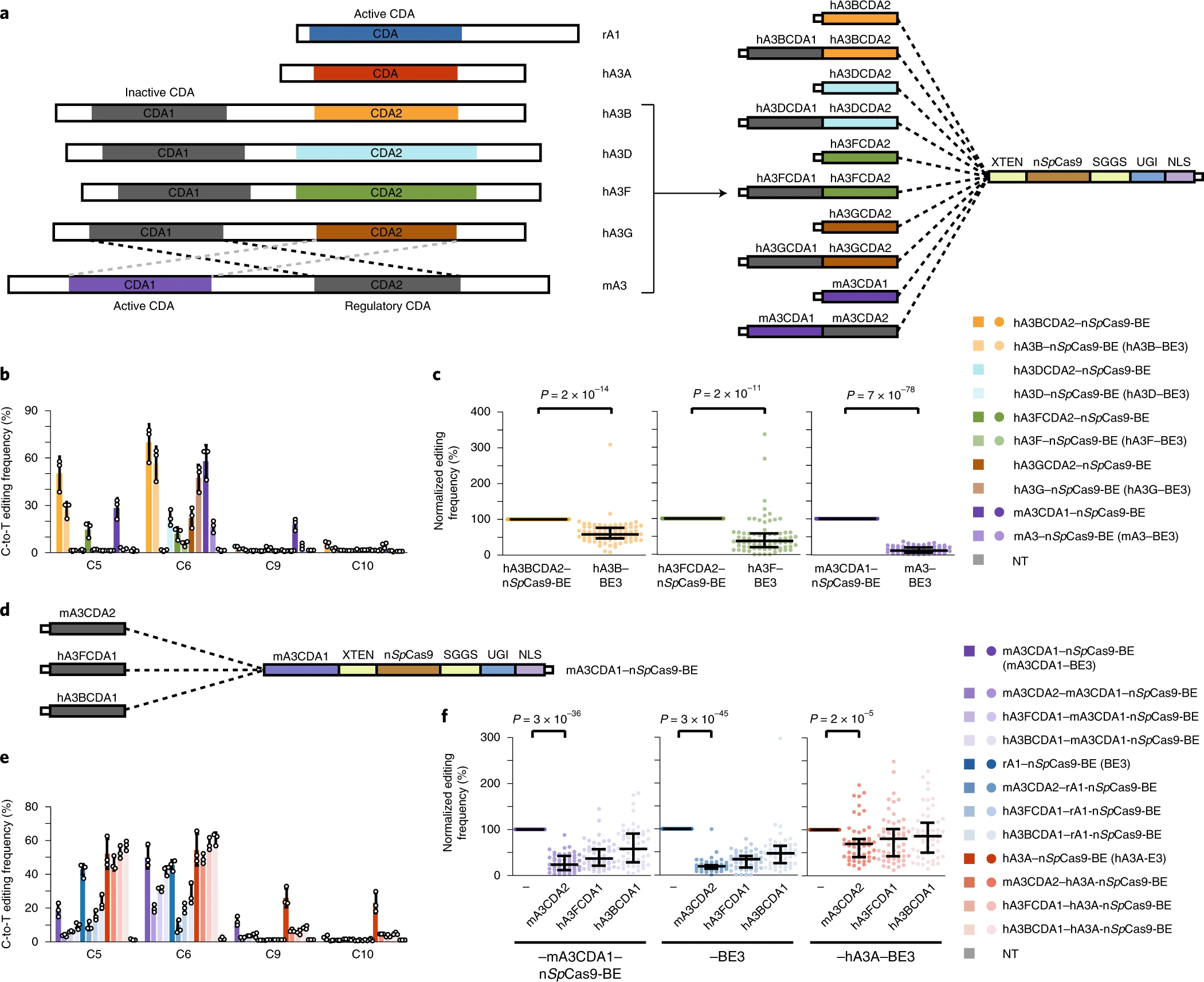
a.APOBEC 家族有两类,一类只有一个CDA 位点,另一类有两个CDA位点,其中一个位点具有催化活性,另一个位点没有催化活性但有调节功能。作者构建了10个BEs,分别包含和不包含inactive but regulatory domain。
b c.包含inactive的CDA位点的APOBEC编辑效率显著降低。
def.为了验证一般性,作者将mA3, hA3F 和 hA3B的inactive CDA位点连接到了mA3CDA1–BE3上,发现都有编辑效率降低。CDA2 of mA3的抑制效果最强。
综上所述,这些调控域作为dCDIs对脱氧胞苷脱氨酶活性具有普遍的抑制作用。
Fig. 2 | Comparison of tBE with other BEs.
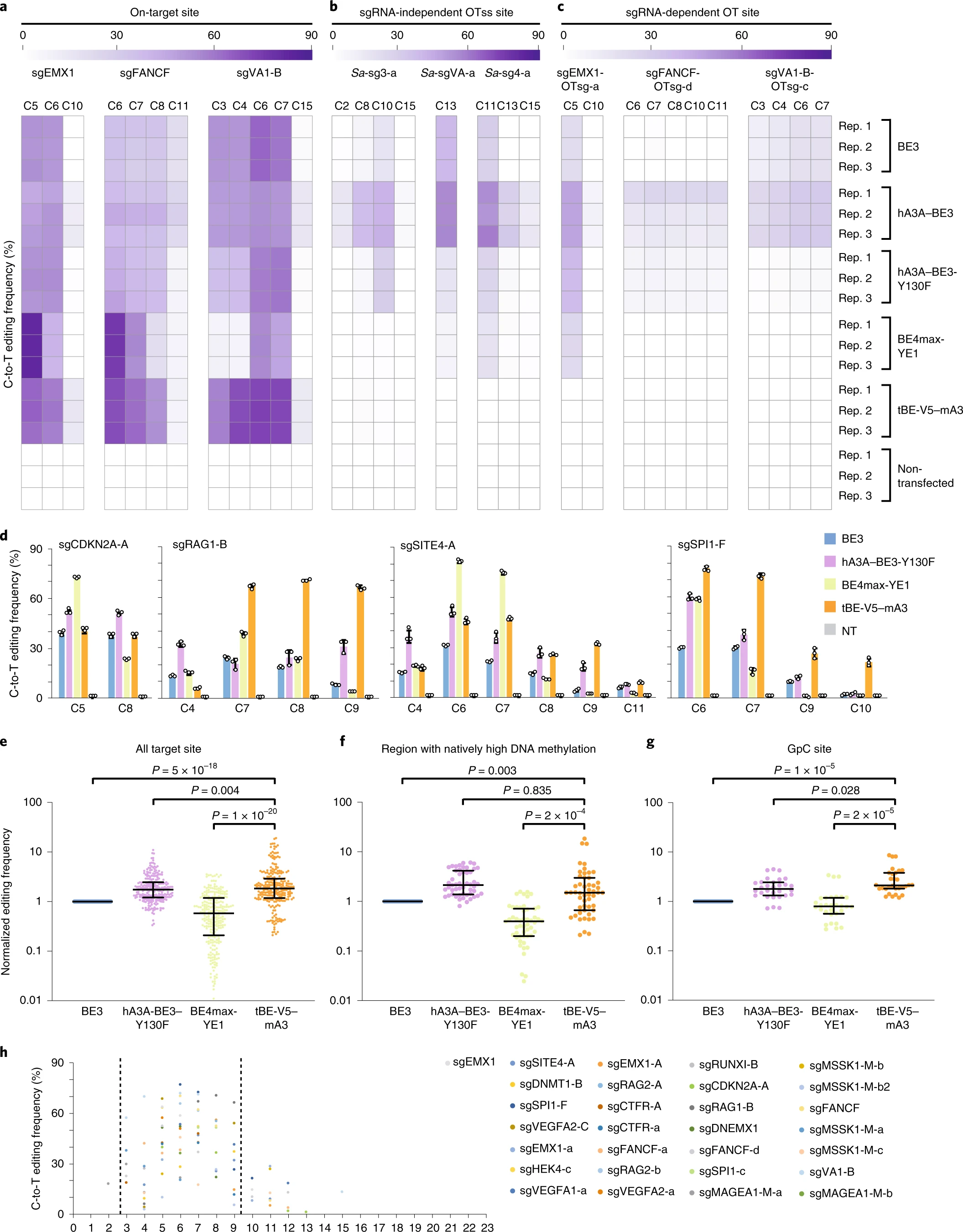
作者试图利用dCDI域开发一个BE系统来避免sgRNA不依赖的突变。理想情况下,由于dCDI的连接,这种BE不会引起可观察到的OT突变,但当与靶点结合时,可以通过切断dCDI而转化为活性;因此被称为tBE。
作者构建了 tBE-V5–mA3 这一BE,并将其与其他的BE进行对比,发现 tBE-V5–mA3 上靶效果很好,包括 DNA甲基化水平高的位点和含GpC二核苷酸 的位点。并且在OTss sites 和 OT sites,只有背景水平的突变。
Fig. 3 | optimization of hsgRNA in the tBE system.
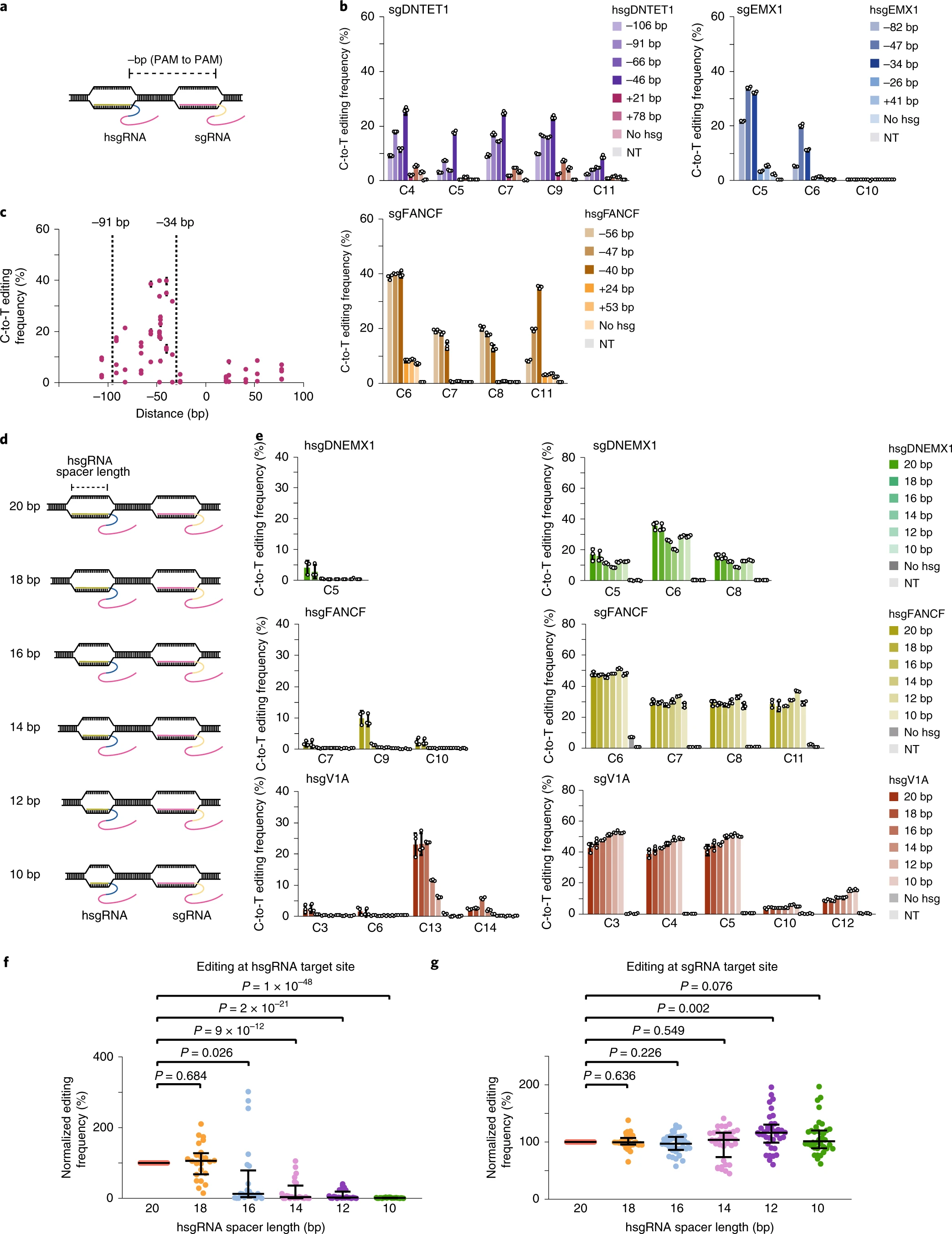
在比较编辑效率时,作者注意到sgRNA和hsgRNA之间的距离影响了tBE对目标的编辑效率。因此,作者测定了sgRNA与hsgRNA之间距离的影响(图3a、b),发现当hsgRNA位于sgRNA的−91 bp至−34 bp(上游)区域时,tBE的编辑效率达到最佳(图3c)
由于hsgRNA在其结合位点也形成R-loop区域(图3d),一些hsgRNA的靶位点偶尔会发生意外的C-to-T编辑 (图3e left)。 之前的研究表明使用带有截断间隔的guide RNA并不影响Cas9的结合 。 因此,作者研究了hsgRNA靶位点的非预期编辑是否也可以通过截断的hsgRNAs来抑制。 使用截断的hsgRNA时,hsgRNA靶区的非预期编辑减少 (Fig. 3e,f). 有10bp间隔的hsgRNA消除了意外的编辑 ,而目标编辑不受影响 。
Fig. 4 | the effect of split-TEV protease concentration on editing efficiency and sgRNA-independent OT mutation.

作者还用不同数量的表达载体表达了分裂- tev系统(图4a),发现在分裂- tev组分检测的蛋白水平上,目标编辑效率(图4b)和sgrna独立OTss位点的突变频率(图4c)均未受影响(图4d)。